Necrobiosis lipoídica diabeticorum:
Descripción y manejo

Néstor P. Sánchez, MD, FAAD
Profesor de Dermatología y Patología
Escuela de Medicina, Universidad de Puerto Rico
Profesor de Dermatología y Dermatopatología
Ponce Health Sciences University
Consultor, Hospital Menonita, Aibonito
Priscilla M. Rosa Nieves, MS3
Ponce Health Sciences University
Génesis Vega García, MS3
Ponce Health Sciences University
Katinna Rodríguez Baisi, MD
Ponce Health Sciences University
Introducción y aspectos históricos
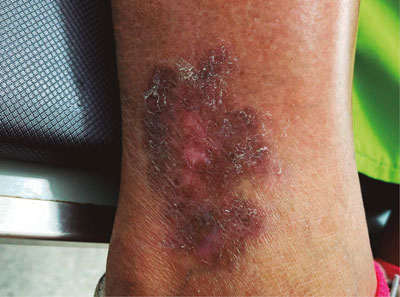
La necrobiosis lipoídica diabeticorum (NLD) es una condición cutánea, crónica y granulomatosa poco común, que afecta mayormente a pacientes diabéticos. La NLD fue descrita por primera vez en 1929 por M. Oppenheim y fue originalmente llamada dermatitis atrophicans lipoidica diabetica.1 Las lesiones se suelen presentar en las extremidades inferiores, específicamente en el área pretibial o posterolateral (Figura 1).2 Se estima que un 15% de las lesiones se desarrollan en áreas atípicas del cuerpo como los antebrazos, la cara, el pecho y el cuero cabelludo.1-3 La NLD puede surgir también en pacientes no diabéticos y fue identificada por primera vez en un paciente sin diabetes en 1935.1
Epidemiología
La NLD tiene una prevalencia del 0.3% al 1.2% en pacientes diabéticos.2 Entre 11% y 35% de pacientes de NLD tienen diabetes mellitus o prediabetes. De los pacientes diabéticos con NLD, un 50% dependen de insulina. La NLD ocurre hasta 3 veces con mayor frecuencia en mujeres que en hombres. La media en edad de inicio de la enfermedad es de 30 años en pacientes diabéticos y de 41 años en los no diabéticos.3 La mayoría de los pacientes sin diabetes que sufren de NLD tienen un historial familiar de diabetes mellitus. Además, distintos estudios sugieren que hasta un 90% de los pacientes no diabéticos desarrollarán diabetes mellitus o tendrán una prueba anormal de tolerancia a la glucosa dentro de los 5 años luego de presentar las lesiones cutáneas.4,5 Por ende, se deben considerar estudios adicionales para la diabetes, de estar indicado, en aquellos pacientes no diabéticos que presentan lesiones de NLD.
Etiología de NLD
La NLD se caracteriza por ser un trastorno cutáneo en el cual degenera el colágeno, dando paso al desarrollo de una reacción granulomatosa. Aunque aún no se conoce bien su etiología, se ha determinado que existe un engrosamiento de los vasos sanguíneos de la persona afectada, tanto en lesiones activas como en áreas sin lesiones.6 Adicionalmente, se han encontrado depósitos de células inflamatorias, lo cual sugiere la posibilidad de una posible vasculopatía. Uno de los principales factores de riesgo es fumar cigarrillos, pues esto aumenta la probabilidad de desarrollar la enfermedad. Esta condición también se ha asociado al carcinoma de células escamosas, especialmente cuando las lesiones son crónicas. Además, se encontró una asociación con condiciones tiroideas en hasta un 25% de los pacientes con NLD. Del mismo modo, se han reportado asociaciones entre NLD y sarcoidosis, artritis reumatoide, enfermedad inflamatoria intestinal, enfermedad de Crohn, colitis ulcerativa, granuloma anular, entre otras patologías.5,7
Patogénesis
La patogénesis de NLD aún no se ha podido comprobar, pero existen varias teorías. La más aceptada es la de microangiopatía diabética. Esta teoría se basa en la deposición de glicoproteínas en las paredes de los vasos sanguíneos (vista en histopatología). Adicionalmente, las inmunoglobulinas pueden ocasionar una vasculitis que pudiera causar cambios en los vasos sanguíneos y eventualmente una muerte celular aislada, llamada necrobiosis. Por otro lado, también se ha considerado el rol de un aumento en los retículos del colágeno, incrementando, a su vez, el grosor de la membrana basal afectada. Otra teoría sobre la patogénesis de la NLD implica trauma, inflamación y cambios metabólicos. Esto interferiría con la migración de neutrófilos y aumentaría la cantidad de macrófagos presentes en el tejido. Por último, se ha considerado también como posible explicación una disfunción en el transporte de glucosa por los fibroblastos.1
Histopatología
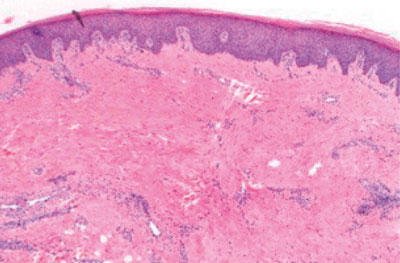
La histopatología de la NLD se caracteriza en sus primeras etapas por un proceso inflamatorio que alterna bandas horizontales de células inflamatorias, mayormente compuestas de neutrófilos, con bandas fibróticas. Este infiltrado inflamatorio, de carácter granulomatoso, involucra toda la dermis y puede extenderse hasta la grasa subcutánea produciendo una paniculitis septal (Figura 2). Las lesiones a nivel de subcutis tienen presentación similar a la dermis, mientras que la epidermis suele mantenerse normal, excepto cuando hay ulceración presente.5
Los hallazgos de inmunofluorescencia en NLD han sido inconclusos y controversiales.8 Los mismos evidencian rasgos clínicos de vasculopatía como, por ejemplo, deposiciones de IgM, C3, IgG e IgA en las paredes vasculares presentes, tanto en las lesiones como en vasos en áreas clínicamente normales. Sin embargo, los pacientes con NLD no muestran otras características necesarias para hacer dicho diagnóstico de vasculopatía.5 Por otro lado, las biopsias intralesionales han demostrado alteraciones en el colágeno dermal y expresión de Glut-1 en estas áreas escleróticas, lo cual sugiere que el transporte defectuoso de glucosa contribuye a los cambios patológicos observados.9,10
Manifestaciones clínicas
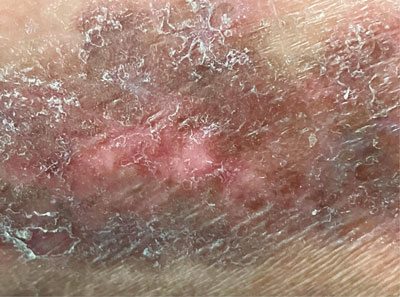
La NLD se presenta primero como pápulas pequeñas y firmes de color variable entre amarillo, marrón y rojizo (Figura 3). Las placas son telangiectásicas, con un borde violáceo elevado7, y pueden progresar a tener una apariencia brillosa parecida a la porcelana.1 Es común que estas lesiones sean singulares o múltiples y pueden ser bilaterales. Además, pueden extenderse y eventualmente desarrollar atrofia epidermal central que pudiera evolucionar a ulceración en aproximadamente un tercio de las lesiones.7 La piel de pacientes con NLD también puede presentar el fenómeno de Koebner, es decir, desarrollar nuevas lesiones patológicas en piel que no está afectada clínicamente por la enfermedad, al enfrentarse a un trauma.2,11
Las lesiones de la NLD pueden resolverse espontáneamente.12 No obstante, pueden convertirse en lesiones persistentes y crónicas. Es aquí donde mayormente vemos complicaciones. La más común es la ulceración, vista en hasta un 30% de las placas. Estas corren el riesgo de infectarse si no son tratadas adecuadamente. También se han reportado complicaciones más severas como, por ejemplo, amputaciones por ulceraciones incesantes, neuropatía periférica, retinopatía y cáncer de piel (específicamente, el carcinoma de células escamosas).1,3,9
Diagnóstico diferencial
Entre las opciones de diagnóstico diferencial están:
- Granuloma annulare (manchas de Binkley): se caracteriza por pápulas de color piel con una forma anular que normalmente tienen una distribución acral y pueden medir de 1 a 5 cm en diámetro. Suele afectar a niños y mujeres menores de 30 años;
- Sarcoidosis: se diferencia por lesiones cutáneas de color rosado y áreas de despigmentación blancas;
- Xantogranuloma necrobiótico: se manifiesta como xantomas eruptivos, tuberosos y tendinosos. En histología se ven hendiduras de colesterol;1 y
- Otras: fibrosis postraumática, morfea, dermatitis por estasis, ectima, nódulo reumatoide, paniculitis, lúes terciarios y tuberculides.3
Tratamiento
Al desconocerse la patogénesis exacta de la NLD, no existe un tratamiento con guías específicas basadas en evidencia. De hecho, la enfermedad suele ser resistente al tratamiento. Sin embargo, se ha reportado remisión espontánea en un 20% de los pacientes.7
A pesar de no existir una relación entre la NLD y el control glucémico, hay casos en los que un control efectivo de la hiperglucemia mejora las lesiones. Posibles explicaciones a esto incluyen:
a. Reversión de microangiopatía y reticulación de colágeno inducidas originalmente por hiperglucemia;
b. Disminución de inflamación y de cantidad de macrófagos; y
c. Normalización del transporte de glucosa por los fibroblastos.1
Entre los medicamentos comúnmente utilizados para tratar la NLD, se encuentran los corticosteroides, inhibidores de plaquetas, potenciadores de cicatrización, inmunomoduladores, entre otros.1 A continuación, explicamos cada uno de estos:
- Corticosteroides: los esteroides orales o tópicos se utilizan para disminuir la inflamación en lesiones activas, pero no deben ser usados en lesiones atrofiadas pues pueden empeorarlas;
- Inhibidores de plaquetas: se ha reportado que la aspirina de 80 mg y el dipiridamol de 75 mg mejoran las úlceras en un periodo de 2 a 4 semanas. En las lesiones sin ulceraciones no hay ningún cambio al utilizar estos medicamentos;
- Potenciadores de cicatrización de heridas: se han reportados casos exitosos usando preparaciones tópicas de factores de crecimiento estimulantes de granulocitos y macrófagos. Estos promueven la cicatrización de las úlceras, favoreciendo su resolución;
- Inmunomoduladores: son los medicamentos más recientemente estudiados y han reportado resultados prometedores. Se han utilizado ciclosporina y mofetil micofenolato en lesiones ulceradas, este último específicamente en pacientes no diabéticos. Infliximab e inhibidores de alfa-TNF se han utilizado en los casos en que ningún otro medicamento ha sido exitoso; y
- Otros medicamentos: en este grupo se incluyen la nicotinamida, la clofazimina, la cloroquina y la tretinoína tópica.1
Comentario
La NLD es una enfermedad dermatológica que se diagnostica principalmente en pacientes diabéticos o con alta probabilidad de desarrollar diabetes mellitus. Aunque no existe un régimen de tratamiento específico, las terapias comúnmente usadas son los esteroides, los inmunosupresores, los inhibidores de plaquetas, entre otros. Las lesiones también pueden resolverse espontáneamente, pero es de suma importancia mantenerlas en observación para evitar ulceración y transformación maligna.12
Referencias
- Kota SK, Jammula S, Kota SK, et al. Necrobiosis lipoidica diabeticorum: A case-based review of literature. Indian journal of endocrinology and metabolism. Pub.: July 2012. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3401767/.
- Lepe K. Necrobiosis lipoidica. National Center for Biotechnology Information. Pub.: Jan 7, 2021. https://www.ncbi.nlm.nih.gov/books/NBK459318/?report=printable.
- Muller S. Necrobiosis lipoidica Diabeticorum. Archives of Dermatology. 1966; 93(3):272.
- Sina B, Kauffman CL. Not all Necrobiosis is Necrobiosis Lipoidica. J Cutaneous Pathol. 2006;33(8):593-593.
- Peyrí J, Moreno A, Marcoval J. Necrobiosis lipoidica. Seminars in Cutaneous Medicine and Surgery. 2007;26(2):87-89.
- Barnes CJ. Necrobiosis lipoidica. Practice Essentials, Etiology, Epidemiology. https://emedicine.medscape.com/article/1103467-overview#a1. Pub.: April 3, 2021.
- Korber A, Dissemond J. Necrobiosis lipoidica diabeticorum. Canadian Med Assoc J. 2007;177(12):1498-1498.
- Dahl MV. Immunofluorescence, Necrobiosis Lipoidica, and blood vessels. Arch Dermatol. 1988;124(9):1417.
- Boulton AJM, Cutfield RG, Abouganem D, et al. Necrobiosis lipoidica Diabeticorum. J Am Acad Dermatol. 1988;18(3):530-537.
- Holland C, Givens V, Smoller BR. Expression of the human erythrocyte glucose transporter glut-1 in areas of sclerotic collagen in necrobiosis lipoidica. J Cutaneous Pathol. 2001;28(6):287-290.
- Gebauer K, Armstrong M. Koebner phenomenon with necrobiosis lipoidica diabeticorum. Internat J Dermatol. 1993;32(12):895-896.
- Reid SD, Ladizinski B, Lee K, Baibergenova A, Alavi A. Update on necrobiosis lipoidica. J Americ Acad Dermatol. 2013;69(5):783-791.








