Genética en el cáncer y su impacto en las nuevas terapias:
Aspectos básicos de un campo en continua evolución

Especial para Galenus Revista para los médicos de Puerto Rico
Adaptado de National Cancer Institute (NCI)
Centers for Disease Control and Prevention (CDC)
American Cancer Society (ACS)
Cambios genéticos y cáncer
Los genes son la unidad física básica de la herencia y se organizan en los cromosomas –que son largas hebras compuestas por ácido desoxirribonucleico (ADN) –. Los genes son los que determinan la forma como crecen y se dividen las células de nuestro cuerpo y están condicionados para llevar instrucciones relacionadas con la producción de proteínas, que son responsables del trabajo a nivel celular.
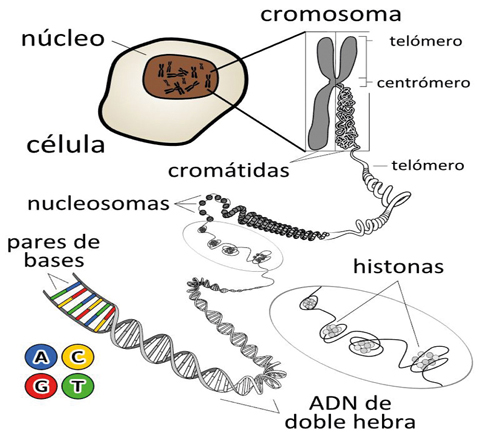
En algunos casos se ha podido determinar en forma concreta que la causa de una enfermedad maligna o cáncer se debe a alguna alteración a nivel de los genes. Así, al ocurrir algunos cambios en los genes, estos pueden llevar a que las células pierdan el control de su desarrollo o de su crecimiento y, de esa manera, se vuelvan cancerosas.
Este tipo de alteración se puede apreciar en los siguientes dos ejemplos: en el caso de que los cambios lleven al aumento descontrolado de la producción de una proteína que hace que las células aumenten de tamaño o cuando se produce una proteína diferente que no es funcional y que, por lo mismo, no contribuye a reparar un daño celular tal como lo haría la proteína original.
Algunos de los cambios genéticos relacionados con el cáncer los podemos heredar en los casos en que estén presentes en las células reproductoras o germinativas –en los óvulos o los espermatozoides– que son las células de la descendencia. Por otro lado, los cambios genéticos causantes del cáncer pueden también presentarse durante la vida con los errores que pueden ocurrir en el ADN cuando las células se dividen o cuando son expuestas a algunas sustancias o elementos que pueden producir un daño, como por ejemplo sustancias en el humo del tabaco o la radiación –inclusive los rayos ultravioletas del sol–. Estos cambios que ocurren después de la concepción son los llamados cambios somáticos (o adquiridos).
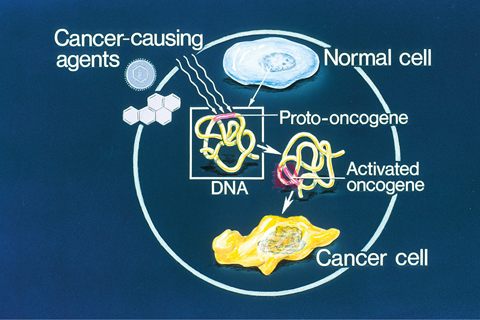
De lo expuesto, se desprenden tres denominaciones a tener en cuenta en relación con los genes y el cáncer:
- Oncogenes: son genes anormales o activados, que proceden de la mutación de un alelo de un gen normal (llamado este protooncogén). De esa manera, los oncogenes son los responsables de la transformación de una célula normal a una maligna, la cual desarrollará algún tipo de cáncer determinado. Se han secuenciado ya decenas de oncogenes;
- Gen supresor tumoral: es un gen que reduce la probabilidad de que una célula se transforme en una célula cancerosa. Los genes supresores de tumores se encuentran en las células normales y generalmente inhiben la proliferación celular excesiva. Una mutación o la deleción de un gen supresor tumoral puede aumentar la probabilidad de que se produzca un tumor, al perder su función. De ese modo, un gen supresor tumoral alterado es similar a un oncogén;
- Genes reparadores del ADN; estos reparan los errores que se producen regularmente durante la transcripción del ADN. Algunos de ellos funcionan como genes supresores de tumores, como ocurre con BRCA1, BRCA2 o p53, que son genes de reparación de ADN.
Los cambios en la estructura del ADN pueden ocurrir en diferentes formas. Pueden verse en el nucleótido –cuando falta o cuando ha sido reemplazado– o comprometer partes más amplias o segmentos –en forma de eliminaciones, duplicaciones o reordenamientos–. Otras veces no afectan la secuencia del ADN, sino que ocurren a nivel del ARN mensajero, que cumple un rol en la producción de las proteínas codificadas.
Adicionalmente, las células cancerosas en general tienen más cambios genéticos que las células normales. En este aspecto suele haber combinaciones únicas para cada persona. Así, conforme avanza el cáncer, pueden también ocurrir cambios adicionales. Inclusive, dentro de un tumor pueden ocurrir cambios genéticos.
Ejemplos de terapias dirigidas a genes
Para ilustrar la repercusión de estos avances –y solo a modo de ejemplos–, mencionamos a continuación algunos productos que ya se vienen utilizando.
En 2017, la FDA aprobó un anticuerpo (pembrolizumab) para tratar a pacientes con tumores metastásicos o no extirpables, que tenían a nivel genético dificultad para reparar los daños en su ADN (por deficiencias conocidas como IMS-A o MMR) surgiendo mutaciones en su estructura genética que producen proteínas anormales. A su vez, estas facilitan a las células inmunitarias a encontrar y atacar el tumor.
Desde 2018, la FDA también ha aprobado el larotrectinib y el entrectinib, ambos medicamentos dirigidos para tratar tumores sólidos que tienen una alteración genética conocida como fusión del gen del receptor de tirosina quinasa neurotrófico (NTRK).
En el mismo año se aprobó otra inmunoterapia, nivolumab, para cáncer colorrectal metastásico (con IMS-A o MMR) que la quimioterapia no había podido detener.
En los tumores pulmonares, las mutaciones genéticas más comunes responsables del cáncer son MYC, BCL2 y p53 para cáncer de células pequeñas (SCLC) y EGFR, KRAS y p16 para cáncer pulmonar no microcítico o de células no pequeñas (non-small cell lung cancer -NSCLC). Sin embargo, hay muchas más alteraciones que pueden estar involucradas en el cáncer pulmonar. Así, otro ejemplo en el que se aprecia la importancia del estudio genético en cáncer se puede ver en NSCLC avanzado o con metástasis, positivo a una fusión genética RET –alteración que se detecta con un kit aprobado por FDA–. Las alteraciones RET ocurren en cerca del 2% de los NSCLC, pero también en cáncer de otros órganos como en el 10-20% de los cánceres de tiroides papilares y en la mayoría de los cánceres de tiroides medulares. Cerca de la mitad de los cánceres positivos de fusión RET hacen metástasis al cerebro. Conocer esto favorece el uso de terapias como selpercatinib o pralsetinib, que son inhibidores de la alteración RET, hacia donde van dirigidos. Así, vemos que el enfoque del tratamiento toma en cuenta, además del órgano, la alteración genética relacionada con el tumor –que en estos últimos casos tiene una mayor importancia–.
Síndromes hereditarios de cáncer
En un 5 a un 10% de todos los cánceres las mutaciones genéticas son determinantes. Los estudios han demostrado que existen relaciones entre algunas mutaciones genéticas y otros tantos síndromes hereditarios de susceptibilidad al cáncer, habiéndose determinado esto en más de 50 tipos de cánceres. Estos síndromes son enfermedades que pueden predisponer a que ocurra el cáncer en las personas afectadas. Sin embargo, desde el punto de vista práctico, aún se discute cuándo se puede recomendar hacer pruebas genéticas para definir si una persona dentro de una familia tiene alguna de esas alteraciones o mutaciones. En general, se recomienda considerar una prueba genética si sus resultados se pueden interpretar con seguridad y si dan información que pueda orientar a una atención médica eficaz y oportuna.
Se debe considerar que tener una mutación familiar que predispone al cáncer no significa que quienes la tengan van a padecer el cáncer, ya que hay varios factores que pueden influir. Además, algunos cánceres no causados por mutaciones genéticas heredadas pueden dar la impresión de que hay una tendencia familiar, lo que más bien puede tener su causa en haber vivido en el mismo ambiente o en haber tenido el mismo estilo de vida.
Algunos ejemplos de los síndromes hereditarios de susceptibilidad o predisposición al cáncer pueden ser:
- La mutación del gen TP53 es la más común en todos los cánceres. Este gen produce una proteína que inhibe el crecimiento tumoral y, al no producirla, pueden aparecer los tumores;
- Las mutaciones en los genes BRCA1 y BRCA2 se asocian con el síndrome hereditario de cáncer de seno y de ovario. Se han asociado también a otros tipos de cáncer, como los cánceres de páncreas y de próstata, así como el cáncer de seno masculino; o
- El gen PTEN produce una proteína inhibidora del crecimiento de tumores. Su mutación (síndrome de Cowden) puede aumentar el riesgo de cáncer de seno, de tiroides, de endometrio y de otros tipos.
Comentario
Con las nuevas tecnologías y también con las alternativas terapéuticas cada vez más precisas, se hace cada vez más válido el considerar la posibilidad de realizar un estudio genético en algunos tipos de cáncer. De acuerdo a la experiencia del médico tratante y del oncólogo en particular, se tomará la mejor decisión.
Referencias
- American Cancer Society: Cancer Facts and Figures 2022. American Cancer Society, 2022.
- Cancer risks in BRCA2 mutation carriers. The Breast Cancer Linkage Consortium. J Natl Cancer Inst 91 (15): 1310-6, 1999.
- Wellcome Trust Case Control Consortium. Nature. 2007. 447: 661-78. .
- The International HapMap Consortium: The International HapMap Project. Nature 426 (6968): 789-96, 2003.
- Resta R, Biesecker BB, et al: A new definition of Genetic Counseling. J Genet Couns 15 (2): 77-83, 2006.









