A tres años de COVID-19:
Considerando aspectos inmunológicos

María L. Santaella, MD, FAAAAI
Inmunología Clínica
El primer caso de COVID-19 oficialmente informado a la Organización Mundial de la Salud (OMS/WHO) fue en China en diciembre de 2019. Sin embargo, estudios basados en evidencia molecular demuestran que la entidad emergió entre octubre y noviembre de 2019. Desde entonces, la pérdida de vidas a nivel mundial ha sido alarmante, superando los 6,5 millones de personas (cifra oficial a octubre de 2022) con el agravante de que el número de afectados con secuelas persistentes de la infección (condiciones post COVID) se desconoce.
La proliferación explosiva de casos a nivel mundial llevó a la OMS a clasificar la situación como una pandemia en marzo de 2020. Para fin de septiembre de 2022, la cifra de muertes reportada es la más baja desde la declaración de la pandemia, lo cual se ha interpretado por algunos como un posible indicio del final de la misma.
Afortunadamente, una rápida sucesión de eventos favorables llevó al descubrimiento del agente etiológico (el virus SARS-CoV-2) en enero de 2020, a la publicación del genoma de este virus en febrero de 2020 por investigadores chinos, y a la simultánea creación en Estados Unidos (McLellan, et al.; Universidad de Texas, Austin) de un mapa atómico tridimensional de la estructura molecular de la proteína S (componente en las espigas de la superficie del virus –virus spike protein–). Dicha proteína –un trímero con una región o dominio (domain) RBD (receptor binding domain)– es la que permite al virus asociarse a receptores para la enzima convertidora de angiotensina (angiotensin converting enzyme, ACE) presentes en muchas células del cuerpo. La fusión entre el receptor para ACE y el RBD del virus permite el acceso de este a las células del cuerpo. En células con baja densidad de receptores ACE, el virus recluta proteasas para lograr la fusión.
La evolución continua del SARS-CoV-2 a diferentes variantes se debe a los cambios que ocurren en su genoma (ya sea por mutación o por recombinación viral), mayormente en la proteína S. Esas alteraciones aumentan la infectividad del virus. La variante ómicron, identificada en noviembre de 2021, es la predominante en la actualidad y se ha caracterizado por presentar múltiples sustituciones en la estructura de la proteína S. Desde principios de octubre, los casos de COVID-19 están en aumento en varios países de Europa y el síntoma más común es dolor de garganta.
Durante los pasados años, la actividad investigativa ha sido intensa para entender la respuesta del sistema inmunitario a la infección, desarrollar nuevas vacunas, e identificar modalidades terapéuticas de diferentes tipos. En este artículo resumimos estos renglones.
Inmunidad innata e inmunidad adaptativa contra SARS-CoV-2
Numerosos estudios documentan que tanto la inmunidad innata como la adaptativa entran en función tan pronto ocurre la entrada del SARS-CoV-2 a las células, para generar las defensas del organismo a la infección.
La inmunidad innata, constituida tanto por células (granulocitos, monocitos, células dendríticas, macrófagos, células de la serie mieloide, linfocitos T NK, -entre otras) como por mediadores, es la primera línea de defensa contra todo tipo de infecciones virales. Su actividad se inicia con el contacto del virus con las células de la mucosa nasal. Este contacto activa receptores PRRs (pattern recognition receptors) en las superficies de las células del sistema innato, que detectan los componentes del virus e inducen la producción de interferones tipo 1, citocinas y quimiocinas proinflamatorias (mediadores). Estos mediadores, a su vez, activan otras células del sistema inmunitario. El movimiento y la activación de células del sistema innato hacia los tejidos, mediado por quimiocinas y citocinas, debe ocurrir de forma ordenada. Cuando ese proceso es uno descontrolado, puede sobrevenir una descarga tormentosa (cytokine storm) de todos esos mediadores, redundando en daño tisular, como ocurre en los pulmones de algunas personas tras su exposición al SARS-CoV-2.
El SARS-CoV-2 puede contrarrestar la acción de los interferones a distintos niveles e inhibir la síntesis de los mismos. En pacientes de COVID-19 se ha descrito la presencia de autoanticuerpos que bloquean los efectos de algunos interferones y una producción anormal de algunos de estos en diferentes tejidos. Se recalca que los interferones inhiben la replicación viral a nivel intracelular. La expresión de los receptores PRRs y la producción de los mediadores inflamatorios (citocinas, quimiocinas) están reguladas por genes. En la actualidad, se estudian patrones genéticos que pudieran aportar al grado de la severidad clínica de COVID-19. Se ha sugerido que el alelo HLA-B 15:01 de las moléculas HLA clase I se asocia a personas que, aunque se infectan con el virus, permanecen asintomáticas.
El componente adaptativo del sistema inmunitario ha sido el más estudiado en COVID-19, en parte debido al desarrollo y a la administración de las vacunas. La figura 1 demuestra cómo la proteína S, producida tras la vacunación, es reconocida por varias células del sistema de defensa para contener el virus. Este componente del sistema inmunitario guarda la memoria de la proteína S.
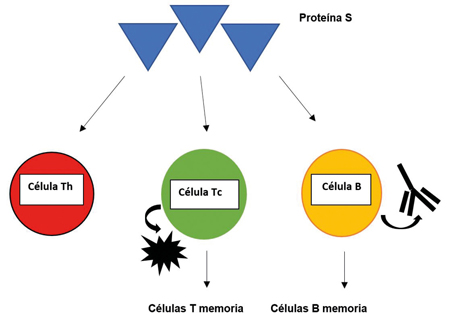
Estudios recientes han demostrado que la población de linfocitos T de memoria puede ser preservada por más tiempo que la población de memoria de los linfocitos B. Esa diferencia ha sido considerada como la explicación para la protección –reflejada en menos hospitalizaciones y en menor severidad de la presentación clínica– observada en personas vacunadas y sin comorbilidades, aun cuando sus niveles de anticuerpos hayan disminuido marcadamente. Se estima que esos linfocitos T de memoria guardan el mensaje de la proteína S para iniciar una respuesta de protección rápida y efectiva de ocurrir una reinfección con el virus.
Se desconoce cómo se organizará la memoria del sistema inmunitario (T y B) a partir de la infección original al encontrarse con nuevas variantes ya sea por infección, por reinfección, por las vacunas o por los refuerzos. Se ha teorizado que el sistema inmunitario pueda conservar su memoria cada vez que se exponga a una variante distinta, creando así un banco de “memorias” del cual pueda suscitarse una respuesta eficiente al encontrar otras variantes subsiguientemente.
Las vacunas
Debido a la identificación continua de mutantes de SARS-CoV-2 y a variantes que pudieran causar preocupación (variants of concern), la implementación de la vacunación es crítica. La meta de las vacunas es producir anticuerpos neutralizantes contra el virus. Las vacunas existentes incluyen: las de virus inactivado, virus vivo atenuado, vectores virales, subunidades proteicas, RNA, DNA, y de partículas parecidas al virus. De las disponibles en los Estados Unidos, con las vacunas de Pfizer y Moderna se inyecta RNA mensajero (material genético del virus); con la de Janssen/Johnson & Johnson (J/JJ), mediante un vector viral se introduce material genético del virus, y con la de Novavax (vacuna de subunidad proteica) se inyectan proteínas S del virus. Todas estas vacunas inducen la actividad de ambos elementos del sistema adaptativo (celular y humoral). Igualmente, conducen a la producción de células de memoria. Los efectos secundarios reportados tras la vacunación han sido mínimos, a excepción de algunos casos de miocarditis. Cabe señalar que la miocarditis es más común tras la infección con el SARS-CoV-2 que tras las vacunas. Se han reportado problemas de trombocitopenia y rara vez de Guillain-Barré (con la vacuna J/JJ).
Actualmente, preocupan dos aspectos de los refuerzos:
- Qué tipo de mensaje se graba en la memoria del sistema inmunitario (immune imprinting); y
- Cuándo es más apropiada su administración.
Sobre 1.: se sabe que el sistema inmunitario sigue produciendo anticuerpos relacionados con la estructura del antígeno inicial, aun cuando reencuentra el mismo antígeno modificado. Ha surgido alguna preocupación por el efecto del material genético de las variantes nuevas en los refuerzos (variantes BA.4 y BA.5) y acerca de que el sistema inmunitario pueda seguir produciendo de preferencia anticuerpos contra la variante original. A pesar de esto, la expectativa sigue siendo que los anticuerpos generados sean efectivos para el efecto deseado: menos hospitalizaciones y muertes.
Sobre 2.: se trabaja en elaborar pruebas de anticuerpos de segunda generación que puedan determinar los niveles de anticuerpos neutralizantes –en bajos, medianos o altos–. Con esta información, se podrían programar los refuerzos individualmente. Sin embargo, aún faltaría estudiar la condición del componente celular –sistema de linfocitos T– para sincronizar los refuerzos.
Ciertas modalidades noveles de vacunas y/o vías de administración están bajo investigación:
- 1. Inoculación mixta (dos tipos de vacunas);
- Vacunas de nanopartículas (parecen ofrecer más protección contra variantes y una respuesta de anticuerpos más sostenida);
- Vacunas con mejores adyuvantes (sustancias que refuerzan la respuesta inmunitaria); y
- Administración por la vía nasal, que aumentaría la efectividad de la respuesta inmunitaria a nivel local (mucosa) y propiciaría una mayor receptividad de las personas para ponerse los refuerzos.
Sobre la vía nasal de inmunización, no se ha estudiado rigurosamente el aporte de la inmunoglobulina A (IgA) en la respuesta inmunitaria contra SARS-CoV-2. La IgA es el anticuerpo predominante en las mucosas, lugar de entrada del virus. Como barrera inmunológica, la IgA secretoria puede neutralizar el RBD antes de que tenga acceso al receptor ACE en las células epiteliales. En un estudio con pacientes con deficiencia de IgA, el riesgo de COVID-19 severo fue 7.7 veces mayor que en personas sin esa condición.
Modalidades terapéuticas
La FDA ha agilizado terapias bajo investigación durante la pandemia a base de acceso expandido (EA) y autorización para uso de emergencia (EUA). La lista es interminable: agentes antivirales, anticuerpos monoclonales, plasma de personas convalecientes, inmunomoduladores (inmunoglobulinas del SARS-CoV-2, corticosteroides, inhibidores de quinasas, de citocinas, de colchicina) y células madre, entre otros.
Para una presentación completa sobre las formas de tratamiento para COVID-19 –existentes y en investigación– se puede referir a las Guías para el Tratamiento de COVID-19 de NIH (Institutos Nacionales de Salud) bajo ese título, actualizadas a agosto de 2022. Estas guías las redactaron expertos de diversas disciplinas, de múltiples entidades públicas y privadas.
Respecto al uso de agentes antivirales, la FDA autorizó, a fines de 2021 dos medicamentos: nirmatrelvir con ritonavir (Paxlovid®) y molnupiravir (Lagevrio®). Ambos son recomendados para personas con un alto riesgo de COVID-19 complicado. Con el primero se han encontrado pruebas positivas de antígeno y/o PCR y la reaparición de síntomas de 2 a 8 días luego de haber terminado el tratamiento de 5 días. Para esa recaída, los Centros para el Control y Prevención de Enfermedades (CDC) recomiendan regresar al aislamiento por 5 días adicionales y continuar con mascarilla hasta 10 días post inicio de los síntomas de la recaída. Se ha informado que el medicamento disminuye en un 73% las hospitalizaciones en un 79% la mortalidad en mayores de 65 años. La recaída puede ocurrir también tras la infección natural y sin el uso de nirmatrelvir con ritonavir (Paxlovid®).
Comentario
Se menciona que ya estamos cerca del final de la pandemia; sin embargo, no existe métrica ni definición específica a nivel internacional para hacer tal aseveración. Algunos opinan que el fin es cuando las personas lo decidan; otros aseguran que es cuando los efectos de la entidad –física y psicológicamente– sean insignificantes. Lo cierto es que, ante la incertidumbre, no se deben hacer pronunciamientos que desalienten a ponerse los refuerzos –sobre todo en personas mayores de 65 años– ni obviar medidas preventivas en ambientes de hacinamiento. Corresponde a la OMS dar el aviso, mientras que el Departamento de Salud y Servicios Humanos de los Estados Unidos estará a cargo de levantar el estado de emergencia con la antelación debida.
Ante la inseguridad de que pueda venir otra ola por otra variante, la investigación debe continuar para:
- Dilucidar los mecanismos de interacción entre el virus y el sistema inmunitario, sobre todo, cómo se conserva la memoria viral en el organismo y cuál es la aportación de la inmunidad en las mucosas;
- Lograr una vacuna efectiva de administración anual;
- Identificar modalidades terapéuticas para erradicar el virus; y
- Afinar los efectos de los refuerzos mediante estudios en humanos enfatizando si estos tienen algún impacto en la incidencia de COVID prolongado (condiciones post COVID).
Referencias
- Wu F, Zhao B, Chen YM. et al. A new coronavirus associated with human respiratory disease in China. Nature 579, 3 Feb. 2020: 265.
- Wrapp D, Wang N, et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science. 2020. 367(6483):p 1260.
- Hoffmann M, Weber HK, Schroeder S, et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell 181(2) 2020: 271.
- Schultze J, Aschenbrenner A. COVID-19 and the human innate immune system. Cell 184(7) 2021: 1671.
- Augusto DG, Yusufali T, et al. HLA-B 15:01 is associated with asymptomatic SARS-CoV-2 infection. PMC 8142661. 2021. medRxiv.
- Sette A, Crotty S. Adaptive immunity to SARS-CoV-2 and COVID-19. Cell 184(4) 2021: 861.
- Li M, Wang H, et al. COVID-19 vaccine development: milestones, lessons and prospects. Signal Transduct Target Ther 7: 2022: 146.
- Jung MK, Jeong SD, et al. BNT162b2-induced memory T cells respond to the Omicron variant with preserved polyfunctionality. Nature Microbiol 7 2022: 909.
- Delgado JF, Vidal-Pla M, Moya MC, et al. SARS-CoV-2 spike protein vaccine-induced imprinting reduces nucleocapsid protein antibody response in SARS-CoV-2 infection. J Immunol Res. 2022: 8287087.
- Colkesen F, Kandemir B, et al. Relationship between selective IgA deficiency and COVID-19 prognosis. Jpn J Infect Dis 75(3) 2022: 228.
- COVID-19 Treatment Guidelines. NIH, updated August 2022.








